Протокол лечения острого лимфобластного лейкоза у детей

Лечение острого лимфобластного лейкоза у детей. Прогноз
Самый главный фактор прогноза при остром лимфобластном лейкозе у детей — лечение, поскольку при отсутствии эффективной терапии больной обречен на смерть. В связи с последними достижениями химиотерапии выживаемость детей с ОЛЛ значительно повысилась.
Лечение зависит от предполагаемого риска рецидива, различного в зависимости от варианта ОЛЛ. К наиболее важным факторам прогноза относят возраст больного при постановке диагноза, исходный уровень лейкоцитов периферической крови и скорость развития эффекта лечения (иными словами, скорость удаления бластных клеток из костного мозга и крови). В группу среднего риска относят детей в возрасте 1-10 лет, уровень лимфоцитов которых составляет менее 50 000/мкл, а в группу высокого риска — детей старше 10 лет с исходным уровнем лейкоцитов выше 50 000/мкл.
Последние исследования показали . что больным из группы высокого риска показана высокодозная химиотерапия, причем эффект от ее применения превышает опасность побочных эффектов. Больные с транслокациями t(922) и t(4ll) имеют достаточно высокий риск рецидива опухоли независимо от высокодозной химиотерапии. Ряд клиницистов показали целесообразность повышения дозы химиотерапевтического препарата в случае медленного развития эффекта от лечения.
В настоящее время большинство детей с острым лимфобластным лейкозом (ОЛЛ) участвуют в национальных и международных исследованиях по изучению данной патологии. Первый этап лечения — индукция ремиссии его цель заключается в удалении лейкозных клеток из костного мозга. Обычная схема химиотерапии рассчитана на 4 нед. и состоит из еженедельного введения винкристина, а также кортикостероида (дексаметазон или преднизолон) и аспарагиназы. При наличии аспарагиназы длительного действия достаточно ее однократное введение.
В ряде случаев интратекально вводят метотрексат и/или цитарабин . Больным из группы высокого риска дополнительно назначают даунорубицин 1 раз в неделю. Эта схема лечения позволяет добиться ремиссии в 98 % случаев (ремиссией называют снижение уровня бластных клеток костного мозга до 5 %, а также нормализацию уровня нейтрофилов и тромбоцитов в течение 4-5 нед.
Второй этап лечения направлен на профилактику поздних рецидивов со стороны ЦНС периодическое интратекальное введение препаратов сочетается с интенсивной системной химиотерапией. В результате второго этапа лечения вероятность поздних рецидивов со стороны ЦНС снижается до 5 %. Некоторым пациентам с высокой вероятностью поражения ЦНС назначают лучевую терапию головного и спинного мозга при наличии лимфобластов или повышенного уровня лейкоцитов в СМЖ при установлении диагноза.
По завершении индукции ремиссии больным назначают полихимиотерапию в течение 14-28 нед. дозы и схемы лечения зависят от группы риска больного. Третий этап длится 2-3 года и носит название поддержание ремиссии. Он состоит из ежедневного применения меркаптопурина и еженедельного введения метотрексата в сочетании с прерывистыми курсами винкристина и кортикостероидов. При наличии у больного неблагоприятных факторов прогноза (например, транслокации t(922) — филадельфийской хромосомы), показана трансплантация костного мозга в период первой Ремиссии. Следует отметить, что филадельфийская хромосома при ОЛЛ напоминает таковую при хроническом миелолейкозе, однако не повторяет ее.
Лечение расценивают как неэффективное в случае рецидива заболевания. Развитие рецидива в костном мозге наблюдают у 15-20 % больных с ОЛЛ. Лечение этих пациентов заключается в назначении нового химиотерапевтического средства с последующей трансплантацией аллогенного костного мозга. Рецидив особенно опасен, если он развивается в процессе химиотерапии либо сразу после нее.
Рецидив острого лимфобластного лейкоза (ОЛЛ) со стороны ЦНС сопровождается повышением ВЧД, а также изолированным поражением черепных нервов. Диагноз подтверждает наличие лейкозных клеток в СМЖ, а также рентгенологическое исследование. Лечение включает интратекальное введение химиопрепаратов и краниоспинальное облучение. В ряде случаев показана системная полихимиотерапия из-за высокого риска рецидива в костном мозге.
Рецидив острого лимфобластного лейкоза со стороны яичек наблюдается у 1-2 % мальчиков и развивается, как правило, после завершения химиотерапии. Клиническое проявление рецидива — безболезненный отек одного или обоих яичек. Лечение включает системную химиотерапию и местное облучение, эффективность его обычно довольно высокая, поэтому выживаемость больных снижена незначительно.
Поддерживающее лечение острого лимфобластного лейкоза
Эффективная терапия острого лимфобластного лейкоза высокими дозами химиотерапевтических средств в большинстве случаев сочетается с поддерживающим лечением. Вероятность развития синдрома распада опухоли у больных с большим объемом опухолевых клеток значительно повышена. Кроме того, тяжелое угнетение кроветворения в процессе химиотерапии требует трансфузии эритроцитной и тромбоцитной массы. Лихорадка у детей с нейтропений служит показанием к неотложному применению антибиотиков широкого спектра действия в высоких дозах. В процессе химиотерапии и нескольких месяцев после нее проводят профилактику пневмоцистной пневмонии.
Новые способы лечения перевели острый лимфобластный лейкоз (ОЛЛ) из разряда острых заболеваний с высокой летальностью в хронические. Вместе с тем длительное лечение влечет не только значительные материальные затраты, но и чрезмерное -нервно-психическое напряжение как больного ребенка, так и его родителей. Кроме того, чем дольше курс лечения, тем выше вероятность побочных эффектов. Опытный гематолог-педиатр должен предвидеть возможные осложнения лечения ОЛЛ, сокращая продолжительность терапии и повышая выживаемость больных.
Прогноз острого лимфобластного лейкоза
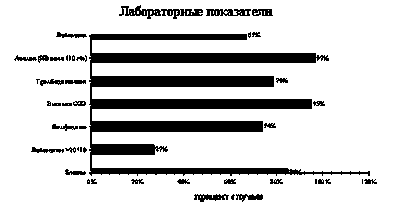
Показатель 5-летней выживаемости детей с острым лимфобластным лейкозом (ОЛЛ) в настоящее время составляет более 80%. Наиболее значимыми факторами прогноза служат выбор оптимальной терапии в зависимости от варианта лейкоза, стадия заболевания, возраст больного, а также скорость развития эффекта после начального лечения. К неблагоприятным факторам прогноза относятся возраст ребенка в дебюте болезни до 1 года или более 10 лет, уровень лейкоцитов более 100 000 в 1 мкл, а также медленное развитие эффекта от лечения. Крайне неблагоприятный прогноз отмечают у больных с недостаточным набором хромосом, наличием филадельфийской хромосомы или транслокацией t(4ll).
При наличии таких признаков . как избыточный набор хромосом, перестройка генов TEL/AML1, а также в случае быстрого развития эффекта лечения прогноз более благоприятный.
Каталог статей
Современное лечение острого лимфобластного лейкоза
ОСТРЫЕ ЛИМФОБЛАСТНЫЕ ЛЕЙКОЗЫ
Острые лимфобластные лейкозы — самые частые злокачественные опухоли у детей, составляют 1/3 всех злокачественных опухолей детского возраста (30 случаев на 1 млн жителей с пиком заболевания в 2—5 лет).
ОЛЛ у детей и взрослых — разные по биологическим признакам заболевания.
Прогноз у взрослых пациентов значительно хуже по сравнению с детьми. 5-летняя безрецидивная выживаемость взрослых больных ОЛЛ на фоне стандартной XT не превышает 25—30%, дети излечиваются в 75—80% случаев.
Классификация.
ФАБ классификация ОЛЛ основана на морфологии бластных клеток: L1, L2, L3.
L1 — бласты мелкие однотипные, цитоплазма узкая, ядро гомогенное, округлое
L2 — гетерогенные клетки больших размеров, цитоплазма умеренно обильная, базофильная, ядро часто неправильной формы
L3 — однотипные клетки крупных размеров, цитоплазма умеренно обильная.
Иммунологическая классификации.
В-ОЛЛ:
1) ранний пре-В (npo-B-ALL или пре-пре В)
2) пре-В (Common, c-pre-B-ALL)
3) зрелый-В-ОЛЛ.
Т-ОЛЛ:
1) ранние Т-ALL
2) тимические (кортикальные) T-ALL
3) зрелые T-ALL.
Подтипы ОЛЛ различаются по клиническим проявлениям, прогнозу, ответу на терапию.
К неблагоприятным по прогнозу иммунологическим подтипам относятся рго-В, Common(c) Ph+, ранние Т-ОЛЛ и зрелые Т-ОЛЛ.
В настоящее время существует молекулярно биологическая классификация ОЛЛ.
Клинические проявления ОЛЛ, как и ОМЛ складываются из клиники синдромов: анемического, геморрагического, интоксикации.
Однако, в отличие от ОМЛ, имеют место проявления, характерные именно для ОЛЛ, такие как инфильтрация яичек и яичников у детей, нейролейкемия, увеличение медиастинальных лимфоузлов при Т-ОЛЛ.
Диагностика основывается на морфологии бластных клеток, цитохимии бластов, иммунофенотипировании, цитогенетическом и молекулярно-биологическом исследовании.
Для ОЛЛ, характерны отрицательная миелопероксидаза, отрицательная липаза, хлорацетатэстераза положительная диффузная PAS-реакция.
Для более точной верификации ОЛЛ в соответствии с иммунологической классификацией необходимо иммунофенотипирование бластных клеток.
Для раннего пре-В-ОЛЛ характерны экспрессия CD19, отсутствие CD 10, clg, slg. Пре-В-ОЛЛ (или Common) характеризуется появлением CD 10, В-ОЛЛ — clg Т-ОЛЛ - CD7, CD3, CD4,8.
Во многих случаях ОЛЛ имеют место хромосомные поломки, определяющие прогноз заболевания и терапевтическую тактику.
В настоящее время выявлено более 40 цитогенетических аномалий.
Самой неблагоприятной хромосомной поломкой является Ph-хромосома (белок р-190) с химерным геном bcr/abl/
У взрослых Ph+ встречается в 25—30% случаев, из них в 40-50% при пре-В-ОЛЛ (Common) варианте.
К благоприятным хромосомным поломкам, определяющим хороший ответ на терапию и излечение, относятся гипердиплоидия (более 50 хромосом) и t(1221). Неблагоприятные хромосомные поломки - t(922), t(4ll), t( 119),
Повышенный цитоз при исследовании ликвора указывает на развитие нейролейкемии.
Рентгенологическое исследование легких помогает выявить увеличение внутригрудных лимфатических узлов и лейкемиды в легких. При проведении УЗИ определяют гепато- и спленомегалию, очаги лейкемоидной инфильтрации в паренхиматозных органах.
Лечение. Тактика лечения ОЛЛ может быть различной. В Европе придерживаются дифференцированного подхода на основании иммунологического варианта ОЛЛ, т.е. существуют разные протоколы лечения в зависимости от варианта и группы риска.
В России для лечения детских ОЛЛ чаше пользуются протоколом BFM, для лечения взрослых пациентов — протоколом D.Hoelzer.
В США используют унифицированный протокол Hyper-CVAD для всех вариантов ОЛЛ у взрослых.
Группа стандартного риска определяется возрастом (1—9 лет), лейкоцитозом менее 50х10*9/л на момент диагностики, t(1221), +4, + 10,+17, наличием полной клинико-гематологической ремиссии на 28 день терапии.
Группа высокого риска: возраст старше 9 лет, для взрослых — старше 35 лет, лейкоцитоз выше 50х10*9/л, наличие Филадельфийской хромосомы (Ph+), t(411), гиподиплоидия, поздний ответ на индукционную терапию.
Принципы лечения: полихимиотерапия (индукция, консолидация), поддерживающая терапия, профилактика и лечение нейролейкемии.
Рекомендации GOC (педиатрической группы) по применению индукционной терапии у детей:
• Пациенты стандартной группы риска получают 3-компонентную индукционную XT с использованием винкристина, преднизолона или дексаметазона, L-аспарагиназы.
• Пациенты группы высокого риска получают 4-компонентную индукционную XT с добавлением антрациклинов или 5-компанентную XT (с добавлением антрациклинов и циклофосфамида).
• Для детей с Т-ОЛЛ — 4-компонентная индукция с преднизолоном.
• На 28 день — стандартизация риска в зависимости от ответа на терапию.
• Пациенты с Ph+ и гиплодиплоидией расцениваются как очень высокий риск.
• Пациенты с реанжировкой гена MLL и транслокацией t(411) и медленным ответом также расцениваются как очень высокий риск.
• Пациенты с быстрым и средним ответом получают консолидацию по протоколам стандартного и высокого риска в зависимости от иммунологического варианта ОЛЛ.
• Пациенты с очень медленным ответом получают дополнительно индукционную терапию в течение 2 недель с оценкой на 42 день.
Рекомендации NCI по терапии и профилактике нейролейкоза у детей. Пациенты группы высокого риска с пре-В-ОЛЛ получают только метотрексат (в подгруппе с ранним ответом на терапию) и метотрексат + + лучевая терапия (в группе с медленным ответом).
В РФ чаше используют триплеты (метотрексат + цитозар + дексаметазон) эндолюмбально.
Использование лучевой терапии для профилактики и лечения нейролейкемии в настоящее время имеет как сторонников, так и противников.
Рекомендации по применению консолидации ремиссии у детей.
В группе стандартного риска — высокодозный метотрексат.
Для детей с антрациклин- или циклофосфанбазисной индукционной терапией рекомендуется поздняя интенсификация спустя 3 месяца после получения ПР.
Критерии, определяющие плохой прогноз у взрослых.
1. Возраст старше 25 или 35 лет.
2. Увеличение уровня b2-микроглобулина.
3. Цитогенетические поломки: Ph+ t(411) без делеции 7 хромосомы трисомия 8 хромосомы.
Дети и взрослые с L3 вариантом ОЛЛ (беркитоподобные, ассоциированные с t(28), t(812), t(822)) лечатся по протоколам для неходжкинских лимфом.
Применение блоковой интенсивной терапии при иммунологически В-зрелом ОЛЛ увеличивает безрецидивную выживаемость с 20 до 60-70%.
Для лечения взрослых с Т-ОЛЛ рекомендуются режимы с циклофосфаном.
У взрослых пациентов использование L-аспарагиназы ограничено в связи с высоким риском развития токсических реакций.
Целесообразность агрессивной постремиссионной терапии доказана только для Т-ОЛЛ.
Не доказана целесообразность агрессивной постремиссионной терапии для пациентов с филадельфийской хромосомой, зрелоклеточных В-ОЛЛ с L3, t(411).
У детей группы стандартного риска ПР достигается в 95% случаев.
Все пациенты ОЛЛ, достигшие ПР, должны получать консолидационную терапию до начала поддерживающей терапии.
Консолидация при ОЛЛ может быть различной средними или высокими дозами метатрексата, использованием препаратов, с помощью которых была достигнута ремиссия, различных комбинаций с малой перекрестной резистентностью к препаратам, использованным в фазе индукции, высокие дозы L-аспарагиназы.
Поддерживающая терапия продолжается от 2 до 3 лет и включает в себя, как правило, метотрексат и 6-меркаптопурин.
Терапия ОЛЛ с Ph+ в настоящее время включает в себя цитостатики и гливек.
Использование гливека при Ph-позитивном ОЛЛ увеличивает частоту ПР с 30% до 90%.
В рамках данной статьи подробное описание всех возможных используемых в настоящее время протоколов для терапии ОЛЛ не представляется возможным.
Эффективность аллогенной трансплантации костного мозга доказана только для пациентов группы очень высокого риска, т. е. ОЛЛ с Ph+.
Для пациентов, не имеющих донора, обсуждается и изучается роль гливека в поддерживающей терапии.
Учитывая отсутствие значительного прогресса в терапии взрослых больных ОЛЛ на фоне стандартной XT, до настоящего времени открытым остается вопрос — все ли взрослые пациенты с диагнозом ОЛЛ и имеющие родственного HLA-совместимого донора должны получать ТГСК в первой ремиссии, или этот метод должен применяться только у пациентов группы высокого риска?
У детей с ОЛЛ Ph+ ТГСК проводится в первой ремиссии, для остальных пациентов — во второй ремиссии.
Прогноз для детей группы стандартного риска — хороший, около 80% излечиваются.
Для детей с ОЛЛ с Филадельфийской хромосомой характерна 10-летняя безрецидивная выживаемость 40-45%, для детей с реанжировкой МLL гена безрецидивная выживаемость еще хуже (35%).
Выживаемость взрослых пациентов с ОЛЛ не превышает 30—35%.
Взрослые пациенты в возрасте менее 30 лет имеют лучший прогноз по сравнению с пациентами от 30 до 59 лет.
Острый лимфобластный лейкоз у детей
Авторы: М.А. Масчан, Н.В. Мякова,
ФГУ Федеральный научно-клинический центр детской гематологии, онкологии и иммунологии МЗ РФ, ФГУ Российская детская клиническая больница МЗ РФ, Москва
Достижения последних десятилетий в области терапии острого лимфобластного лейкоза (ОЛЛ) у детей являются одной из наиболее ярких страниц современной медицины. Принципиальная возможность излечения подавляющего большинства пациентов и их возвращение к полноценной жизни стали, безусловно, главным результатом серии клинических исследований, выполненных на протяжении четырех десятилетий в США и Европе. Методология проведения исследований, разработанная на модели ОЛЛ, остается ориентиром для разработки программ медикаментозной терапии в клинической онкологии. В настоящем обзоре сделана попытка суммировать современные принципы диагностики и терапии ОЛЛ у детей.
Эпидемиология
ОЛЛ – самое распространенное злокачественное заболевание у детей. В структуре педиатрической онкологической патологии доля ОЛЛ составляет до 25% всех опухолей и до 75% всех гемобластозов. Заболеваемость ОЛЛ претерпевает существенные географические вариации, составляя в среднем 30–40 случаев на 1 млн населения в год. Характерной особенностью является так называемый младенческий пик – увеличение заболеваемости ОЛЛ до 75 на млн в год в возрасте от 2 до 5 лет. Более низкая заболеваемость ОЛЛ отмечается в странах Африки и Средней Азии, относительно более высокая – в Китае, Японии, США, Европе. Чаще заболевают мальчики (соотношение 1,6:1 для В-линейного и 4:1 для Т-линейного ОЛЛ). Риск развития ОЛЛ у детей ассоциирован с рядом факторов, наиболее значимыми из которых являются [1, 2]:
Существование множества факторов, находящихся в слабой ассоциации с риском развития ОЛЛ, свидетельствует в пользу модели ОЛЛ как результата сложного взаимодействия полиморфных генетических систем и элементов окружающей среды.
Клиническая характеристика ОЛЛ у детей
Клиническая презентация ОЛЛ у детей весьма вариабельна и обусловлена опухолевой инфильтрацией и нарушением функции пораженных органов [3]. Интоксикационный синдром проявляется астенией, лихорадкой, недомоганием, потерей массы тела и утратой психомоторных навыков у детей раннего возраста.
Дисфункция костного мозга проявляется анемическим синдромом: бледностью, тахикардией, снижением толерантности к физической нагрузке. Геморрагический синдром может быть обусловлен как тромбоцитопенией, так и коагулопатией, особенно при гиперлейкоцитарных вариантах ОЛЛ, и проявляется пурпурой, носовыми и желудочно-кишечными кровотечениями. Лихорадка может быть обусловлена собственно лейкозом или течением бактериальной, вирусной либо грибковой инфекции, особенно у детей с абсолютной нейтропенией. Гиперпластический синдром включает увеличение периферических лимфоузлов в виде пальпируемых плотных безболезненных конгломератов. Инфильтрация печени и селезенки приводит к гепатоспленомегалии и может проявляться болями в животе, увеличением объема живота, тошнотой, анорексией. Лейкемическая инфильтрация надкостницы и суставной капсулы, инфаркты кости и опухолевое увеличение объема костного мозга приводят к развитию болей в костях [4]. При этом на рентгенограммах обнаруживаются характерные изменения, особенно в трубчатых костях, возле крупных суставов. Первым проявлением заболевания могут быть патологические переломы трубчатых костей или позвоночника. Артралгии и отек суставов могут быть ошибочно приняты за симптомы ревматоидного артрита или других заболеваний, а поражение костей – за остеомиелит.
Инициальное увеличение яичек у мальчиков отмечается в 5–30% случаев ОЛЛ это безболезненные, плотные, одно- или двусторонние инфильтраты. Истинная частота поражения яичников у девочек неизвестна, но, по данным некоторых исследований, она составляет от 17 до 35%. Особенно часто это бывает при гиперлейкоцитозе и Т-клеточном варианте ОЛЛ [5]. Известны случаи значительного увеличения почек в результате лейкемической инфильтрации, при этом клинические симптомы поражения почек могут отсутствовать. Редкими осложнениями являются инфильтрация миокарда и выпотной перикардит при обструкции путей лимфооттока между эндокардом и эпикардом.
Таблица 1. Прогностические факторы при ОЛЛ у детей
Что такое острый лимфобластный лейкоз?
Острый лимфобластный лейкоз представляет собой злокачественную патологию системы кроветворения, сопровождающуюся неконтролируемым размножением и увеличением числа лимфобластов – незрелых лимфоидных клеток.
Избыточное число незрелых лимфоцитов образуется в костном мозге, что приводит к вытеснению из ткани здоровых клеток.
Лейкоз поражает практически все органы, распространяясь на центральную нервную систему, зрительный нерв, органы половой системы, легкие. Считается системным злокачественным заболеванием и требует немедленного интенсивного лечения. Острый лимфобластный лейкоз у детей и подростков развивается чаще, чем во взрослом возрасте.
На возраст от года до пяти лет приходится пик заболеваемости. Среди девочек заболеваемость меньше, чем среди мальчиков.
Развитие заболевания у детей обусловлено злокачественным перерождением лимфоцитов, что влечет прекращение развития новых клеток. Процесс остановки развития клеток может произойти на любой стадии клеточного формирования, соответственно ОЛЛ может проявляться различными формами, отличающимися своим течением и требующими различного подхода к терапии.
В-лимфобластный лейкоз более распространен по сравнению с т-формой, встречается чаще всего у детей трехлетнего возраста, когда в организме ребенка происходит активная продукция в костном мозге в-клеток. Т-клеточный лимфобластный лейкоз чаще всего развивается в подростковом возрасте.
Острый лимфобластный лейкоз у взрослых встречается реже, в основном в пожилом возрасте (после 60 лет). Заболевание у взрослых часто сопровождается поражением нервной системы, хуже поддается лечению.
Острый лимфобластный лейкоз у беременных встречается не часто, развивается у женщин, которые болели лейкозом в детстве и при их лечении удалось достигнуть стадии ремиссии. При этом беременность не оказывает влияние на течение болезни. При лейкозе у беременной повышается риск выкидыша, преждевременных родов. Исход беременности определяется эффективностью терапии. Лейкозная инфильтрация тканей плаценты и плода отмечается редко.
Видео: Подробно об остром лимфобластном лейкозе
Причины
Досконально причины острого лимфобластного лейкоза не выявлены. Считается, что на возникновение болезни могут влиять как наследственные, так и внешние факторы.
К факторам риска можно отнести:
Симптомы острого лимфобластного лейкоза
В развитии патологии выделяют 5 этапов:
- предлейкозный период
- обострение заболевания
- период ремиссии
- рецидив
- терминальный период.
Наличие последних двух этапов определяется успешностью лечения: при эффективности терапии они отсутствуют. При первичной резистентности этапы ремиссии чередуются с рецидивами.
Предлейкозный период
Характеризуется отсутствием явных клинических проявлений заболевания и невозможностью диагностики.
Острый период
Начинается стремительно, характеризуется различными клиническими проявлениями с разрастанием злокачественной ткани и функциональным нарушением кроветворения.
Происходит увеличение лимфоузлов, размеров внутренних органов, бластное перерождение костного мозга. У взрослых на этапе обострения болезни отмечается интоксикационный, геморрагический и гиперпластический синдром, анорексия.
Интоксикационный синдром сопровождается общей слабостью, лихорадочным состоянием, снижением веса. Гиперпластический синдром сопровождается увеличением лимфатических узлов (особенно в паховой и подмышечной области, в зоне шеи), болями в животе при увеличении селезенки и печени, болями в костях и суставах, отеками, патологическими переломами, ростом объема костного мозга.
Анемический синдром характеризуется бледностью кожных покровов, слабостью, тахикардией. Геморрагический синдром выражен небольшими либо значительными кровоизлияниями, носовыми, почечными и кишечными кровотечениями.
Рецидив
Рецидив может проявляться следующими нарушениями со стороны внутренних органов:
Такие симптомы, проявляющиеся на начальных этапах болезни, свидетельствуют о неблагоприятном прогнозе.
Диагностика
Для подтверждения/исключения диагноза проводятся следующие исследования:
- общий анализ крови
- исследование костномозговой пункции
- исследование спинномозговой пункции
- ультразвуковое исследование и рентгенография органов брюшной полости
- биохимический анализ крови.
Дифференциальная диагностика позволяет практически всегда с высокой степенью достоверности выявить заболевание. При постановке диагноза в первую очередь необходимо исключить другие заболевания, сопровождающиеся поражением костного мозга – апластическую анемию, миелофиброз, инфекционный мононуклеоз и прочие.
В этой статье можно узнать подробно о лечении лейкоза в России.
Методы лечения
Лечение острого лимфобластного лейкоза проводится в несколько этапов:
Для лечения острого лимфобластного лейкоза возможно проведение трансплантации костного мозга.
Пересадка осуществляется после достижения стадии ремиссии. При этом важно не допустить присоединения инфекционных процессов, поскольку иммунная система при трансплантации существенно ослаблена. Существуют различные программы лечения ОЛЛ. Выбор той или иной программы основан на разделении пациентов на группы по интенсивности применяемой терапии, скорости ответа на терапию и ожидаемым прогнозам.
Для пациентов, у которых удалось достигнуть ремиссии при использовании умеренной химиотерапии, не должна применяться тяжелая и токсичная терапия. Любой протокол лечения острого лимфобластного лейкоза строится на принципах интенсивной химиотерапии, направленной на разрушение лейкемических клеток.
Симптомы хронического лейкоза у взрослых описаны тут .
Почему дети болеют лейкозом, расскажет статья .
Прогноз (выживаемость)
Острый лимфобластный лейкоз у детей значительно лучше поддается лечению, чем у взрослых.
Так, в детском возрасте пятилетняя ремиссия достигается в 70% случаев. У взрослых же этот показатель составляет лишь 20%.
Заболевание может завершаться совершенно непредсказуемо как при благоприятном течении, так и при сложных формах.
Источники:
, , ,
Следующие статьи:
27 июля 2024 года
Комментариев пока нет!

 Чем лечить кашель у грудного ребенка комаровский
Чем лечить кашель у грудного ребенка комаровский Что дать ребенку от поноса 5 лет
Что дать ребенку от поноса 5 лет Как принимать ацикловир в таблетках при герпесе у детей
Как принимать ацикловир в таблетках при герпесе у детей Чем лечить коньюктивит у ребёнка 1 месяц
Чем лечить коньюктивит у ребёнка 1 месяц Ацикловир капли для глаз детям
Ацикловир капли для глаз детям Показания для назначения ацикловира у детей
Показания для назначения ацикловира у детей